전기화학 에너지 저장 장치에서 전자 전도와 이온 확산은 전극 재료의 성능을 결정하는 데 중요한 역할을 합니다. 리튬 이온 배터리를 예를 들면(그림1), 전자는 외부 회로를 통해 재료의 표면으로 이동하고 이온은 내부 회로를 통해 확산되어 궁극적으로 활성 물질, 전자 및 이온 간에 전기 화학 반응을 일으켜 전기 에너지와 화학 에너지 간의 변환을 가능하게 합니다. 일반적으로 외부 회로에서의 전자 전달은 내부 회로에서의 이온 확산보다 빠릅니다. 따라서 빠른 전하 균형을 달성하고, 재료 표면에 순전하 축적을 방지하며, 빠른 충전-방전 프로세스 중에 분극을 줄이기 위해서는 재료 인터페이스 특성을 지속적으로 개선해야 합니다[1]. 요약하면, 재료 내 이온 확산은 전기화학 반응에서 중요한 반응 과정이자 제한 단계입니다. 이온 확산의 정확한 특성화는 전극 재료의 설계 및 합성을 안내하는 데 가장 중요합니다.
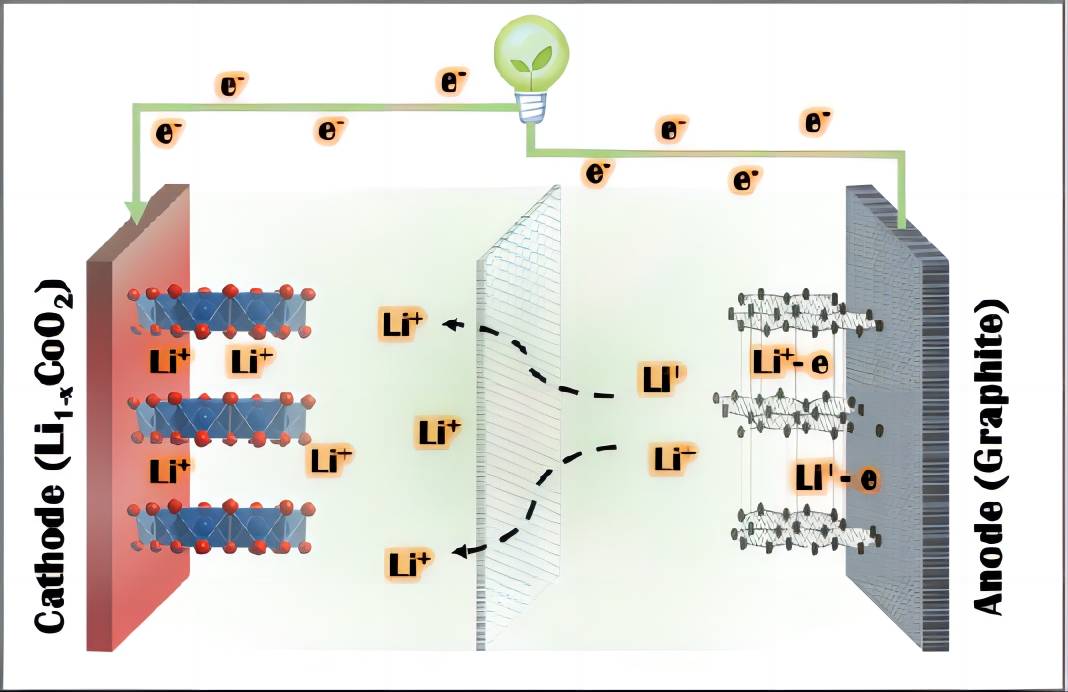
그림1 리튬 이온 배터리에서 전자와 이온의 전도 거동
물질 내 이온 확산은 농도가 높은 영역에서 낮은 영역으로 이온이 이동하여 물질 내 이온 농도가 균질화되는 현상을 말합니다[1]. 이온 확산 속도를 특징짓는 물리적 파라미터는 이온 확산 계수입니다. 이온 확산 계수를 결정하기 위한 일반적인 테스트 방법에는 정전류 간헐적 적정 기법(GITT), 정전기 간헐적 적정 기법(PITT), 순환 전압 측정법(CV), 전기 화학 임피던스 분광법(EIS), 전류 펄스 이완(CPR), 정전기 전류 단계 전류 측정법(PSCA) 및 정전기 이완 기법(PRT) 등이 있습니다. 이 문서에서는 GITT 기술에 중점을 두고 테스트 원리, 방법 및 적용 사례에 대한 자세한 요약을 제공합니다.
정전류 간헐 적정 기술(GITT)은 전위와 시간 간의 관계를 분석하여 반응 동역학에 대한 정보를 얻는 테스트 기법입니다. 독일 과학자 W. 웨프너가 처음 제안했습니다. 완전한 GITT 테스트는 그림 2와 같이 여러 개의 “전류 단계” 단위로 구성됩니다. 각 전류 스텝 단위(그림 3) 내에서 전기화학 시스템은 일정 기간 동안 낮은 전류로 횡방향 충전 및 방전을 받습니다. 그런 다음 인가된 전류가 차단되고 일정 기간이 유지되어 이온이 활성 물질 내에서 완전히 확산되어 평형 상태에 도달할 수 있도록 합니다. 전극 전위와 이완 시간의 변화를 분석하고 이를 활성 물질의 물리화학적 파라미터와 결합하여 물질 내 이온의 확산 계수를 유추하고 계산할 수 있습니다.
GITT 테스트는 이온 확산이 주로 고체상 물질의 표면층에서 발생한다고 가정하므로 인가 전류 시간(t1)과 이완 시간(t2)에 다음과 같은 제약 조건이 적용됩니다.
a) 전류 펄스의 적용 시간(t1)은 충분히 짧아야 하며, 최소한 t1 << L²/D를 만족해야 합니다. 여기서 L은 재료의 특성 길이이고 D는 이온의 확산 계수입니다.
b) 이완 시간(t2)은 안정된 전압을 기준으로 Li+ 이온이 활성 물질 내에서 충분히 확산되어 평형 상태에 도달할 수 있을 만큼 충분히 길어야 합니다.
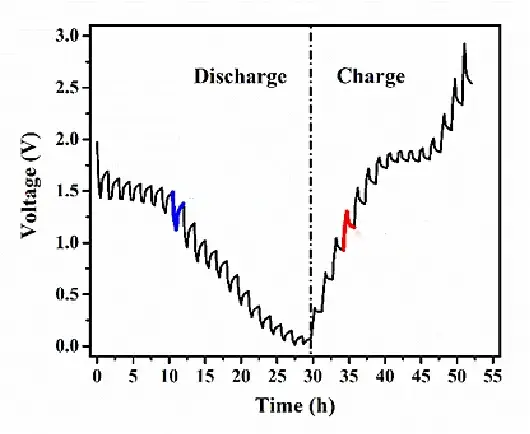
그림 2 완전한 GITT 곡선
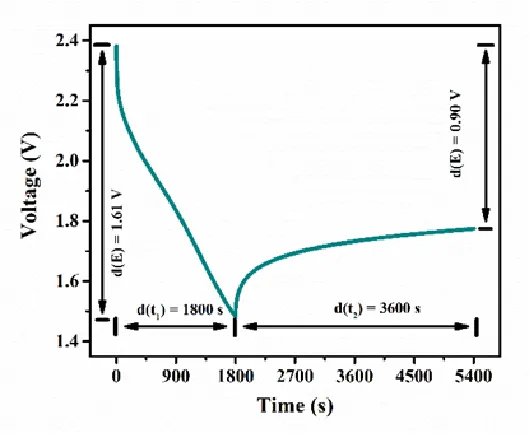
그림 3 전류 단계의 전압 및 시간 곡선
GITT에서 이온 확산 계수를 결정하는 이론적 근거는 Fick의 법칙에서 도출됩니다. 피크의 첫 번째 법칙은 확산 종의 농도가 시간에 따라 변하지 않고 거리에 따라서만 변하는 정상 상태 확산에만 적용되므로 정상 상태와 비정상 상태의 거동을 모두 포함하는 물질 내 리튬 이온의 확산을 완전히 설명할 수 없습니다. 따라서 거리와 시간에 따른 확산 종의 농도 변화를 설명하는 픽의 두 번째 법칙이 사용됩니다.
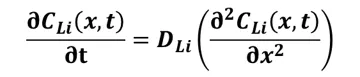
초기 조건, 경계 조건을 통합하고 활성 물질 입자 내의 부피 변화를 무시하면 Fick의 제 2 법칙을 풀어서 확산 계수 D를 구할 수 있습니다.
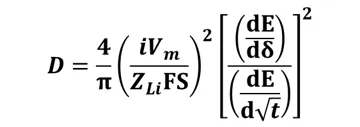
여기서 알려진 파라미터는 i(전류(mA)), Z_(Li-)(리튬 이온의 전하 수, 1), F(패러데이 상수, 96485 C/mol), S(전극/전해질 접촉 면적)이고 미지 파라미터는 dE/dδ(쿨롱 적정 곡선의 기울기) 및 dE/d√t(전위와 시간 간의 관계[2])입니다.
인가 전류가 충분히 작고 이완 시간(τ)이 충분히 짧으면 dE/d√t 사이의 관계가 선형이 되어 계산 공식이 더욱 단순해집니다.
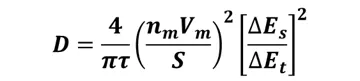
여기서 τ는 이완 시간, n_(m)은 몰 수, V_(m)은 몰 부피, S는 전극/전해질 접촉 면적, ∆E_(s)는 펄스로 인한 총 전압 변화, ∆E_(t)는 정전류 충전/방전 시 전압 변화입니다.
전극에 전류가 흐르는 순간 오믹 저항과 전하 이동 임피던스의 존재로 인해 전극 전위가 급격히 증가/감소한다는 점에 주목할 필요가 있습니다. 이 전체 과정은 일시적인 현상입니다. 그 후 전류가 일정하게 유지되면 전위는 천천히 변화하기 시작합니다. 따라서 그림 4와 같이 충전/방전 중 ∆Et에는 iR로 인한 전압 변화가 포함되지 않습니다. 또한 D의 크기는 이완 시간과 관련이 있음을 알 수 있습니다. 따라서 정확한 테스트 결과를 얻으려면 전극 전위가 본질적으로 변하지 않도록 충분히 긴 이완 시간을 선택해야 합니다.
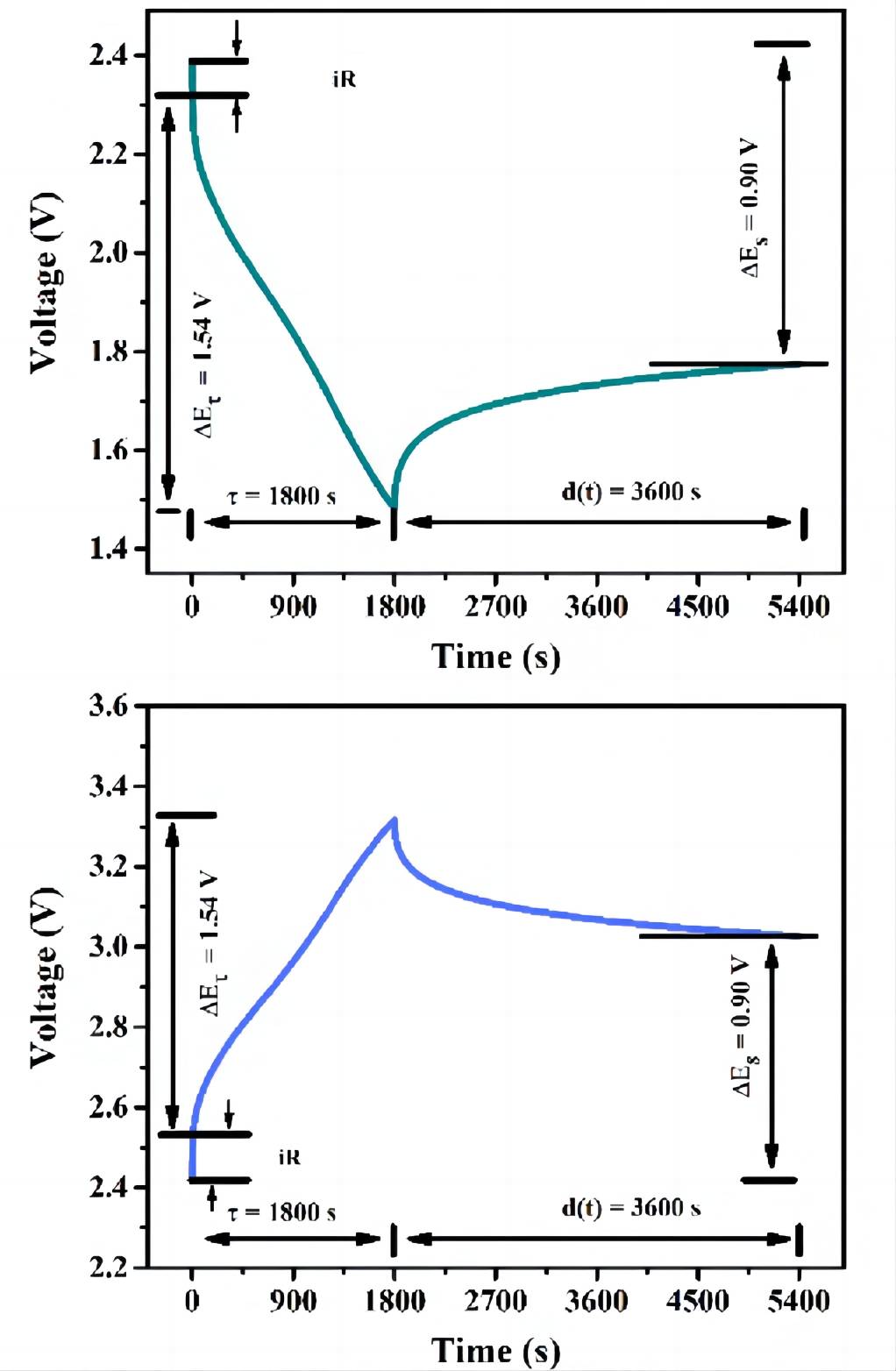
그림4 GITT 곡선의 방전(위)/충전(아래) 중 전류 단계
각 '펄스-이완' 단위의 ∆Es와 ∆Et를 얻음으로써 그림 5와 같이 전체 충-방전 과정에서 전위/충-방전 깊이에 따른 리튬 이온 확산률의 변화를 계산할 수 있습니다.
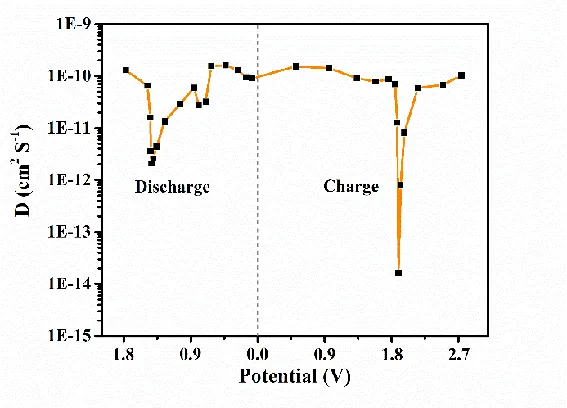
그림 5 다양한 전위에서 리튬 이온의 확산 계수
GITT는 일반적으로 충방전 테스터 또는 전기화학 워크스테이션을 사용하여 수행합니다. NEWARE 정전류 충전-방전 테스터를 예로 들어 GITT 테스트 프로세스를 설명합니다.
(1) NEWARE 정전류 충전-방전 테스터 소프트웨어(그림 6)를 두 번 클릭하여 테스트 인터페이스로 들어갑니다(그림 7).
그림 6 NEWARE 배터리 테스터 소프트웨어-BTS8.0.0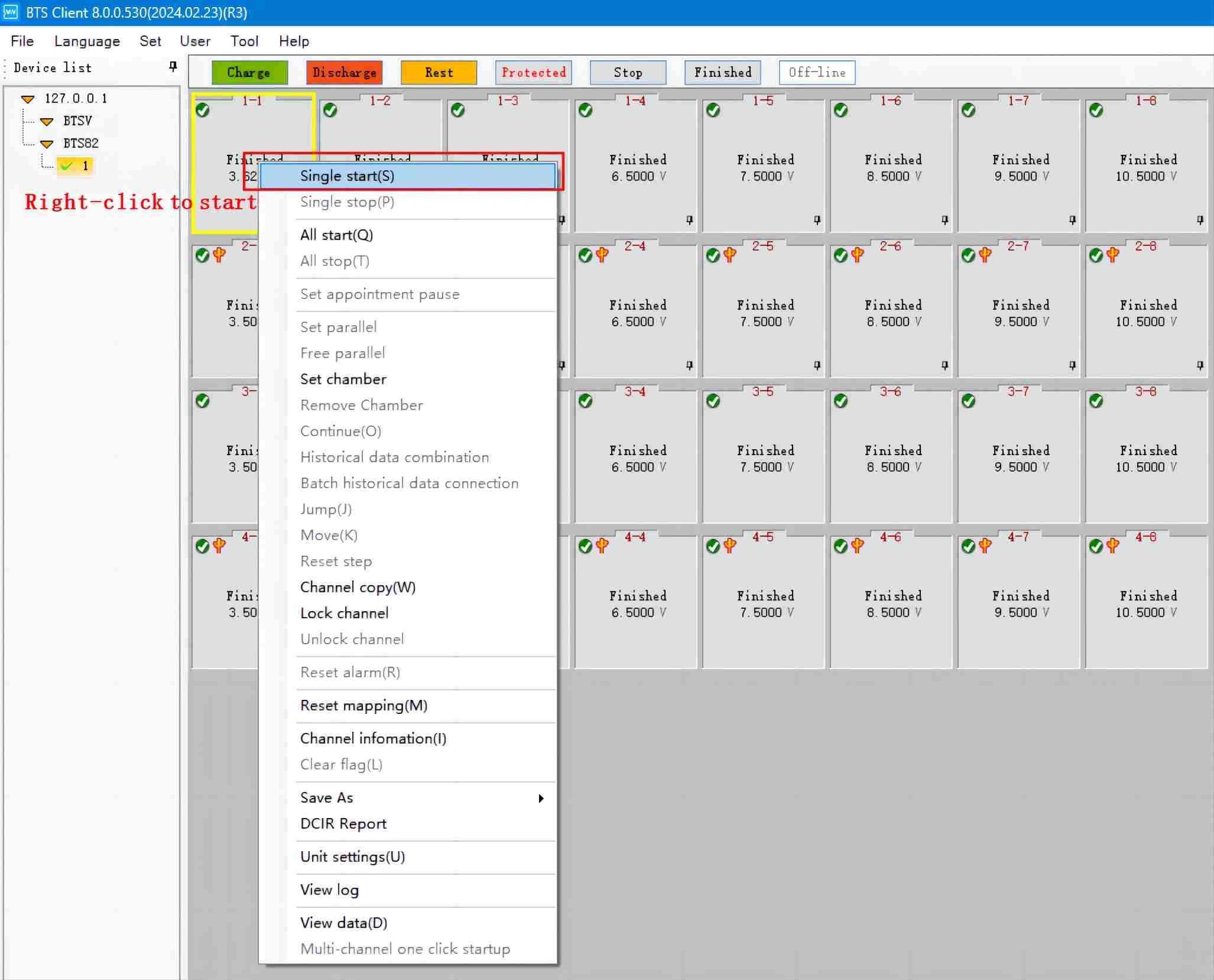
그림 7 NEWARE 정전류 충전 방전 테스터 메인 인터페이스
(2) 테스트 채널을 선택하고 마우스 오른쪽 버튼을 클릭하여 스텝 편집 인터페이스로 들어갑니다. 테스트 절차는 제공된 스텝 테스트 템플릿을 참조할 수 있습니다. GITT 테스트에 사용되는 펄스 정전류는 일반적으로 작으며 0.1C/0.1A의 계산을 선택할 수 있습니다. 펄스 시간은 일반적으로 10~30분 사이로 상대적으로 짧아야 합니다. 확산 시간(이완 시간)은 전압이 본질적으로 더 이상 변하지 않는 상태로 회복될 수 있도록 충분히 길어야 합니다. 그림에 표시된 매개변수 값은 데모용으로만 사용되었습니다. 구체적인 파라미터 값은 실험의 요구 사항에 따라 결정해야 합니다.
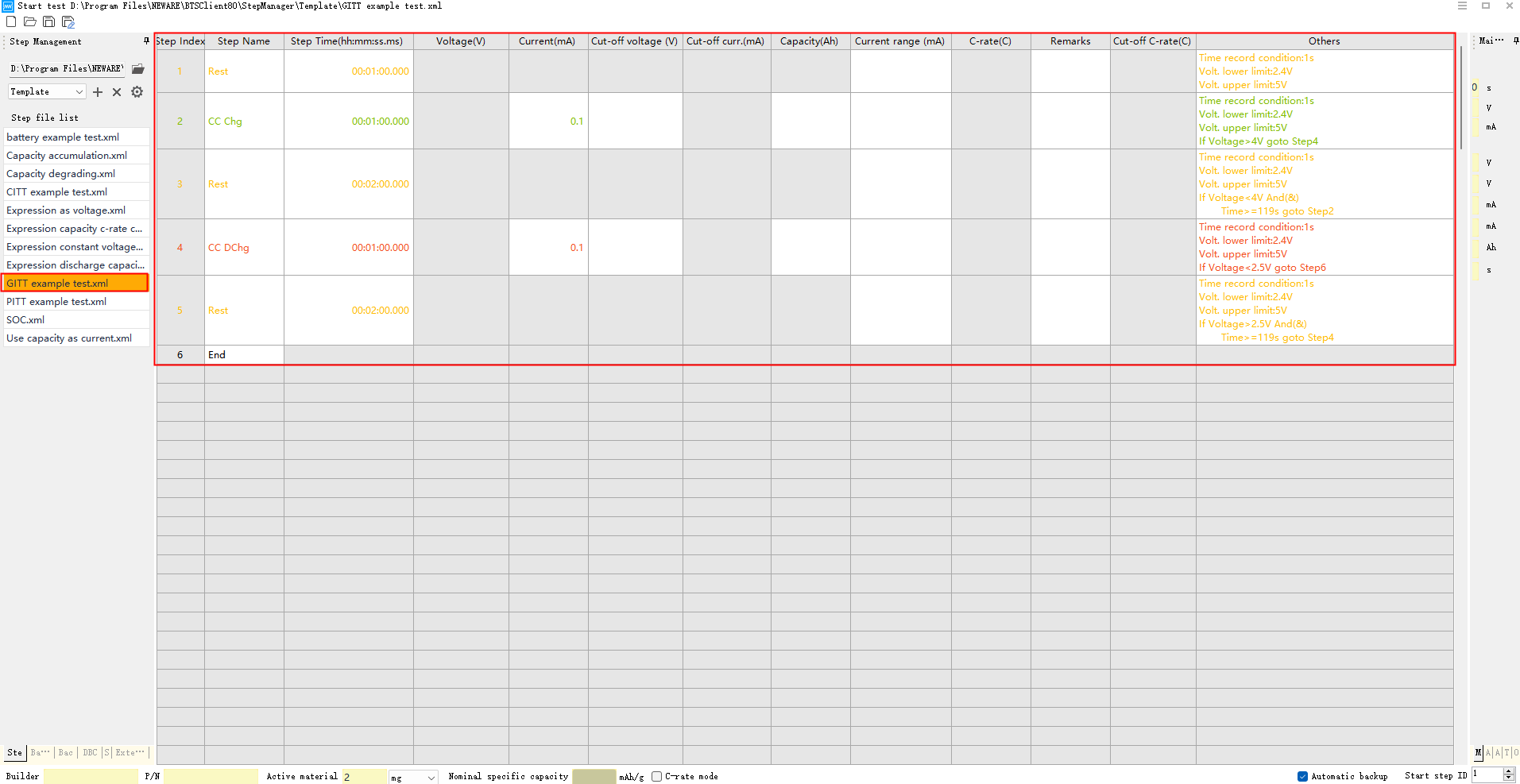
그림 8 일반적인 음극 재료 설정을 위한 GITT 테스트 절차
(3) 테스트 후 데이터는 그림 9와 같습니다.
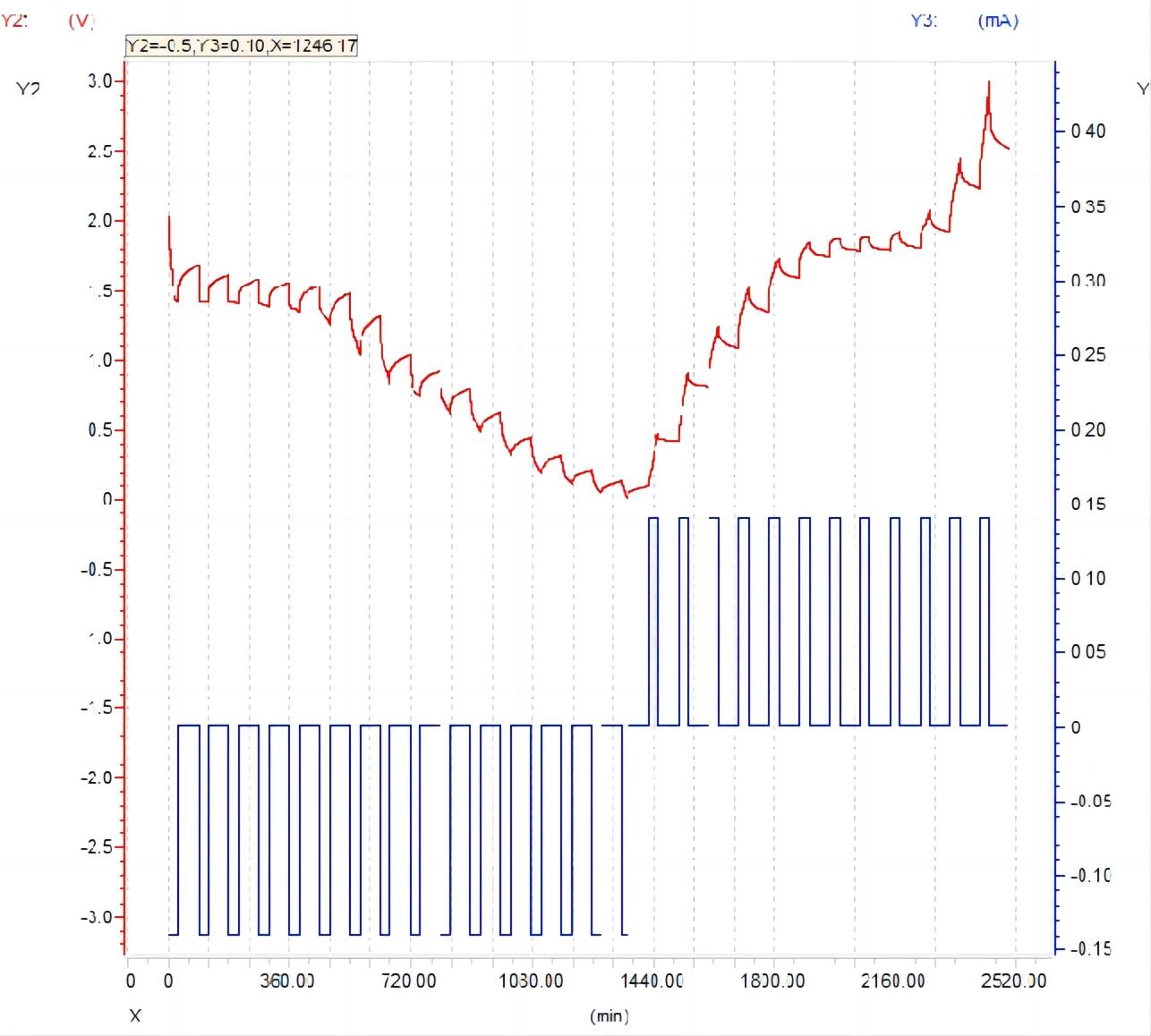
그림 9 GITT 테스트 후 데이터 화면
GITT 테스트의 경우, 먼저 방전할지 충전할지는 정전류 충전-방전 테스트와 일치해야 합니다. 예를 들어 S, V₂O₅ 및 FePO₄ 양극 물질이 Li와 결합된 경우 충전하기 전에 먼저 방전해야 합니다. 따라서 GITT 테스트에서는 충전 전에 방전을 수행해야 합니다.
예 1: 작성자는 새로운 고온 및 고부하 인산철 리튬(UCFR-LFP) 복합 전극을 보고했습니다. 사이클링 및 속도 성능 테스트 결과, 이 전극은 속도 성능과 사이클링 안정성 모두에서 기존의 인산철 리튬 전극(Con-LFP)보다 뛰어난 성능을 보였습니다. GITT 테스트를 통해 UCFR-LFP 전극의 평균 리튬 이온 확산 계수(3.6×10-¹¹ cm² s-¹)가 Con-LFP(5×10-¹² cm² s-¹)보다 훨씬 높다는 사실이 밝혀졌습니다. 다른 구조적 특성과 결합하여 저자는 활성 물질과 전도성 물질 사이의 밀착을 보장하고 전극 전체의 전해질 확산 및 수송을 촉진하며 전극의 전자 및 이온 수송 경로를 최적화하는 UCFR-LFP의 독특한 복합 다공성 구조에 기인할 수 있다고 분석했습니다.
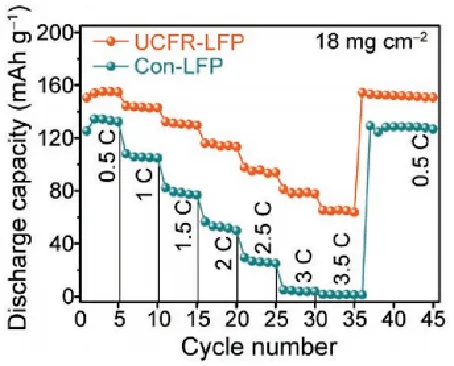
그림 10 두 LFP 전극의 확대 성능 비교[2]
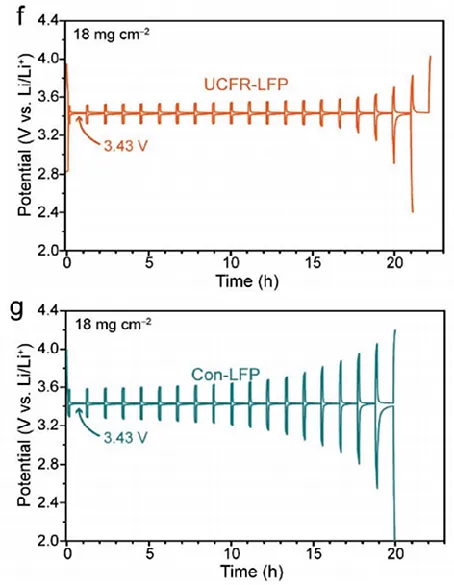
그림 11 두 LFP 전극[3]의 GITT 곡선 비교[3]
예 2: 저자들은 수성 아연 이온 배터리(ZIB)의 양극 재료로 일련의 바나듐 바나데이트 나노 물질을 보고했습니다. GITT 분석을 통해 K₂V₈O₂₁ 및 K_(0.25)V₂O₅와 같은 터널 구조를 가진 바나듐 바나데이트가 아연 이온 확산을 촉진하는 동시에 KV₃O₈ 및 K₂V₆O₁₆-1 층을 형성한다는 사실을 밝혀냈습니다. 구조 붕괴가 일어나기 쉬운 57H₂O는 아연 이온 확산 계수가 낮아 고용량을 달성하기 어려웠습니다.
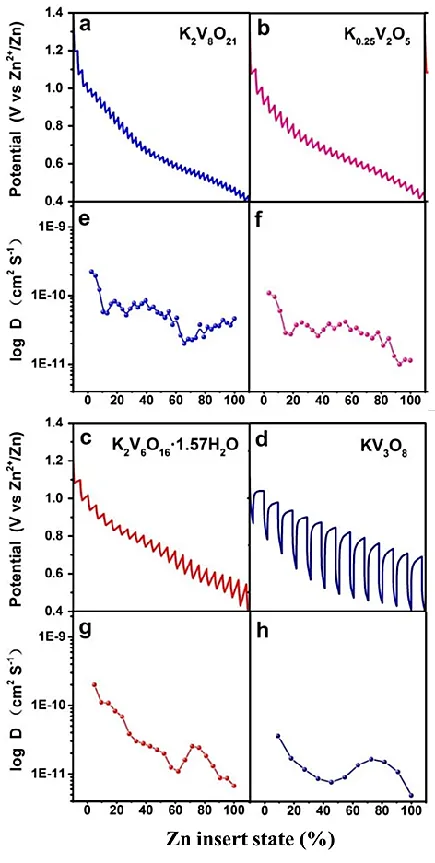
그림 12 네 개의 전극(a-d)과 아연 이온 확산 계수(e-h)에 대한 GITT 곡선[4]
[1].ZHENG Hao, GAO Jian, WANG Shaofei, LI Hong. Fundamental scientific aspects of lithium batteries (VI)--Ionic transport in solids[J]. Energy Storage Science and Technology, 2013, 2(6): 620-635.
[2].LING Shigang, WU Jiaoyang, ZHANG Shu, GAO Jian, WANG Shaofei, LI Hong. Fundamental scientific aspects of lithium ion batteries(ⅫⅠ) —Electrochemical measurement[J]. Energy Storage Science and Technology, 2015, 4(1): 83-103.
[3].Li H, Peng L, Wu D, et al. Ultrahigh-Capacity and Fire-Resistant LiFePO4-Based Composite Cathodes for Advanced Lithium-Ion Batteries[J]. Advanced Energy Materials, 2019, 9(10):1802930.
[4]. Boya T, Guozhao F, Jiang Z, et al. Potassium vanadates with stable structure and fast ion diffusion channel as cathode for rechargeable aqueous zinc-ion batteries[J]. Nano Energy, 2018, 51: 579-587.
Seoul: NEWARE
19th Taerung Techno Town, Gasan-dong, Geumcheon-gu, Seoul 1314, 70 Gasan digital 2-ro, Geumcheon District, Seoul, Korea
(서울특별시 금천구 가산디지털2로 70, 대륭테크노타운19차 1314호)


